第16号 【2026年5月1日等施行】2025年薬機法等改正の全容(概要)(ガバナンスと供給責任の抜本的強化)
文献番号 2026WLJLG004
Westlaw Japan コンテンツ編集部
【この記事のポイント】
- ・経営者層の責任も強化・実効的なガバナンス体制の強化:責任役員変更命令の新設と品質保証責任者等設置の法定化
- ・出荷停止時等の届出義務や安定供給体制整備義務が法定化
- ・創薬アクセスの加速:条件付き承認の拡大による「早期承認・市販後検証」モデルへの一部移行と小児用医薬品開発計画策定等の努力義務化
- ・薬局・販売現場の適正化:外部委託の一部解禁による業務効率化と若年者等による医薬品濫用防止対策の厳格化
Ⅰ 概要
1.改正の必要性
医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律等の一部を改正する法律(令和7年法律第37号)が、2025年5月21日に公布され、一部の経過措置等を除き、同年11月20日以降、段階的に(2026年5月1日等)施行されています。今回の医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(以下「薬機法」とします。)等の改正は、近年の医薬品業界を取り巻く以下のような深刻な課題を解決するために断行されました。
(1)ガバナンスの形骸化と不正の頻発
医薬品メーカー等による相次ぐ不正事案では、現場の法令違反を経営陣が把握していない、あるいは是正できないといった統治不全が浮き彫りとなりました。近年の行政処分事案においては、責任役員の関与があった事案も見られ、従来の法人への業務停止命令等だけでは、不祥事を起こした企業の体質を根本から変えるには限界があったといえるでしょう。そこで、今回の改正では、責任役員の変更命令のような仕組みを導入するなど、より実効的なガバナンス強化を求めるような改正がされました。
(2)医薬品供給不足の常態化
後発医薬品を中心に数年にわたる供給不足が続いていますが、これまでは出荷停止等の報告が企業の自主的な協力に委ねられており、国が迅速かつ正確に需給を把握等する法的権限が不十分でした。そこで、今回の改正では、医療用医薬品等の安定供給体制の強化等に係る改正も行われています。
(3)ドラッグ・ラグ及びドラッグ・ロス解消の必要性
国際的な創薬競争において、日本での開発が遅れる「ドラッグ・ラグ」や、開発自体がなされない「ドラッグ・ロス」が深刻化しており、患者に革新的な医薬品を迅速に届けるための制度的後押しが急務となっています。そこで、今回の改正では、より活発な創薬が行われる環境の整備に係る改正も行われています。
2.改正内容
以下では、令和7年改正(2025年改正)の主要な4つの柱について詳述します。
(1)医薬品等の品質及び安全性の確保の強化
a 責任役員の変更命令権の新設
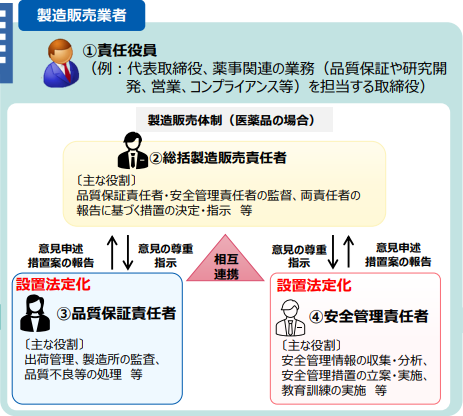
今回の改正で最もインパクトが大きいものの1つは、厚生労働大臣による製造販売業者及び製造業者に対する「責任役員の変更命令」の創設でしょう。本改正では、薬事に関する業務に責任を有する役員(責任役員)が原因で、薬事に関する法令違反が発生し、国民の生命・健康に大きな影響を与える可能性がある場合には、国(厚生労働大臣)が、その責任役員の変更を命じることができるようになりました。コンプライアンス違反が発生した際、特定の役員個人の解任を国から直接迫られるリスクが生じます。本改正の背景には、経営陣が現場の法令違反を把握・是正できていないどころか、不正に関与していた事例等、医薬品等の製造販売業者等の(経営層による)ガバナンスの機能不全が強く疑われる事案が見受けられたことがあります。変更命令の新設自体は、行政権限の強化に関する改正ですが、上記のような背景を踏まえ、実務上は、下記の品質保証責任者等の設置等の体制も含め、医薬品等の品質及び安全性の確保に係る体制を形式だけ整えるのではなく、経営層が実質的に適切に監視できるような体制を整えることが重要です。なお、この変更命令の対象となる責任役員と、その下に置かれる各責任者の位置付けは、以下の図のとおりです。
b 品質保証責任者等の法定化(法律による設置義務化)等
今回の改正では、これまで省令レベルの規定であった医薬品製造販売業者における「品質保証責任者」及び「安全管理責任者」の設置義務を法定し、また、それぞれ変更命令の対象としました。品質保証責任者と安全管理責任者の実施する業務等も薬機法上明確化されたものの、「総括製造販売責任者」の下に「品質保証責任者」と「安全管理責任者」が位置するという従前からの三責構造(上図参照)には大きな変動はありません(「2024年12月26日 令和6年度第10回 厚生科学審議会医薬品医療機器制度部会 議事録」(厚生労働省ウェブサイト)参照)。「品質保証責任者」は、出荷管理等のような医薬品の品質保証の統括を、「安全管理責任者」は、安全管理情報の収集・分析等のような医薬品の安全管理の統括を、各々「総括製造販売責任者」の監督下で行い、各分野の統括に必要な場合には、医薬品総括製造販売責任者に対して書面で意見を述べることが求められ、これにより、安全性や品質に関する経営陣主導の対応が強化されることが期待されます。「総括製造販売責任者」は、両責任者の監督及び両責任者の報告に基づく措置の決定・指示等を行い、両責任者の意見が述べられた場合には、各責任者の意見を尊重しなければなりません。また、「総括製造販売責任者」自身は、医薬品の品質保証及び製造販売後安全管理の統括を公正かつ適正に行うために必要があるときは、製造販売業者に対し、意見を書面により述べなければなりません。もともとこのような体制を整備している企業がほとんどであると思われますが、上記の背景もあることから、この機会に、それぞれの責任者の役割等につき、薬機法等に沿っているか、手順書等のみならず、実際の運用も見直し、全体として、実効的なコンプライアンス違反の疑いがある場合等の報告ルートが整備できているか、改めて確認・検討するのもおすすめです。
c 副作用に係る情報収集等に関する計画(RMP)の作成、実施の義務化
さらに、副作用に係る情報の収集・分析・対応の遅れが重大な問題を引き起こす可能性があることから、医薬品の製造販売業者は、厚生労働大臣が指定する医薬品につき、副作用に係る情報収集等の計画(いわゆるRMP、Risk Management Plan)の作成と実施が義務付けられました。この計画は、品質、有効性及び安全性に関する資料や最新の論文等により得られた知見に基づき、作成、変更することが求められます。また、策定した計画は厚生労働大臣に報告しなければなりませんし、計画を変更する場合も同様です。さらに、その計画に基づく実施状況についても、厚生労働大臣へ報告しなければなりません。従来、RMPの実施は承認条件とされており、法律と全く無関係というものではありませんでした(「2024年12月26日 令和6年度第10回 厚生科学審議会医薬品医療機器制度部会 議事録」(厚生労働省ウェブサイト)参照)が、本改正では承認要件としてではなく、事業者の義務として制定されていることから、実務への影響が少なからず想定されるため、注意が必要です。
上記a~cの改正については、公布の日から2年を超えない範囲(2027年5月20日まで)において政令で定める日に施行されます。
d その他の主な改正事項
医薬品等の品質及び安全性の確保の強化に関しては、上記の他、GMP(Good Manufacturing Practice、医薬品等の製造管理及び品質管理の基準)適合性調査の合理化と監督強化、体外診断用医薬品の特性を踏まえた性能評価等の見直し、医薬品製造管理者等の要件の見直しや国家検定制度の合理化、感染症定期報告制度の合理化、登録認証制度の安定的な運用に向けた見直しに係る改正もなされています。
(2)医療用医薬品等の安定供給体制の強化
特定医薬品の製造販売業者に対して、医療用医薬品の安定供給のための体制整備等に係る義務が課されました。
a 供給体制管理責任者の設置と届出等の義務(平時)
まず、本改正では、新たに、「特定医薬品」が定義されました。「特定医薬品」とは、主として、医療用医薬品を念頭にしたもので、医薬品のうち、要指導医薬品・一般用医薬品・一定の薬局製造販売医薬品等を除いたものです。
本改正では、この特定医薬品の製造販売業者につき、特定医薬品の安定供給体制を整備する観点から、新たに「供給体制管理責任者」の設置が義務付けられました。この「供給体制管理責任者」の業務及び遵守事項は、厚生労働省令で定められますが、おおまかには、「手順書」を踏まえた企業内の体制整備、取組の推進、安定供給に関する法令遵守等を行うことが求められ、また、「手順書」には、安定供給のための社内各部門の連絡調整体制の整備、原薬の確保、在庫管理、生産管理等に関する手順が記載されることが想定されています(「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律等の一部を改正する法律(令和7年法律第37号)の概要」(厚生労働省ウェブサイト)参照)。また、特定医薬品の製造販売業者は、供給体制の整備等を実施することが求められます。上記改正のうち、特定医薬品の定義の策定に関する規定は、2025年11月20日に施行されており、その他の改正は、公布の日から起算して2年を超えない範囲内(2027年5月20日まで)において政令で定める日に施行されます。
また、特定医薬品の製造販売業者は、その製造販売する特定医薬品について、6月以内にその出荷の停止や制限をすることとした又はそのおそれがあると認めるときは、直ちに厚生労働大臣にその旨を報告しなければなりません。さらに、実際に出荷停止や制限をした際には、直ちに厚生労働大臣へ届出が必要です。このような報告や届出により供給不安がある場合、厚生労働大臣は、代替薬の製造販売業者等に報告を求めることができ、その供給状況を把握等することが想定されています。この改正は、2025年11月20日に施行されています。
b 増産等の協力要請・指示の創設(有事)
深刻な供給不足時等には、厚生労働大臣が関係企業に対し、必要な協力を要請、又は場合によっては、指示できるようになりました。具体的には、供給不安等が生じた場合、厚生労働大臣は、製造販売業者に対してその医薬品又は代替薬の増産・販売の調整、薬局開設者や病院診療所の開設者等に対して、調剤や処方に関する配慮等、必要な協力を求めることができます。また、製造販売業者や製造業者は、安定的な供給確保の必要性の高い医薬品として指定する「供給確保医薬品」の中でも、特に重要なものとして指定する「重要供給確保医薬品」につき、場合によっては、「供給不足防止措置計画」や「製造等計画」を、作成し、届け出るよう指示を受けることが想定されます。指示に従い届出をした製造販売業者等は、供給不足防止措置計画に沿って、重要供給確保医薬品等の供給不足の発生を未然に防止するために必要な措置を行う義務、又は製造等計画に沿って、要供給確保医薬品等の製造又は輸入を行う義務を負います。厚生労働大臣は、特に必要があると認められる場合には、計画の変更も指示できます。また、正当な理由なく、指示に従わない場合や計画通りに措置が行われていないと認められる場合、厚生労働大臣はその旨を公表できます。この公表により企業のレピュテーションにダメージを与える可能性があることも踏まえた対応を行うことが重要です。その他、「供給確保医薬品等」の製造販売業者、製造業者、卸売販売業者等には、供給状況の報告義務等も課されるなどの改正も行われています。これにより、実際に供給不足不安等が生じた場合で国民への医薬品の提供困難が解消しやすくなることが期待されます。上記の各改正は、2025年11月20日に施行されています。
なお、後発医薬品産業全体の構造的問題を解決し、品質の確保された医薬品の安定供給を目指す目的で、「後発医薬品製造基盤整備基金」も新たに創設されました。この基金を利用して、生産性向上のための設備整備を行うなどして、品質の確保された医薬品を安定的に供給できるよう、設備面の整備等を行うのも一案でしょう。
(3)より活発な創薬が行われる環境の整備
本改正では、革新的な医薬品の早期実用化や小児用医薬品の開発を促進するなどのためのインセンティブを強化します。
a 条件付き承認制度の見直し
重篤かつ代替する適切な治療法がない疾患に係るものであるなど、医療上の必要性が特に高い医薬品等を対象に、少数の患者を対象とする探索的試験等で臨床的有用性が合理的に予測可能である場合には、承認後に検証的臨床試験等を行うことを条件とする承認が可能となりました。申請に係る効能、効果等を有すると合理的に予測できなくなったなどの場合、この承認は取り消されます。この制度の詳細は、「医薬品の条件付承認の取扱いについて」(厚生労働省ウェブサイト)等も参考になります。上記の改正は2026年5月1日に施行されます。
b 小児用医薬品の開発促進(努力義務)
薬局医薬品の製造販売業者に対して、「小児用の薬局医薬品の開発を促進するために必要な小児の疾病の判断、治療又は予防に使用する医薬品の品質、有効性及び安全性に関する資料の収集に関する計画」(小児用医薬品の開発計画)の策定及び同計画に基づく必要な資料の収集が努力義務とされました。また、小児用医薬品の開発計画が策定された医薬品の再審査の期間が、既に上限(10年)で設定されている場合、最大2年延長できることになりました。上記の改正は2026年5月1日に施行されます。
なお、後発医薬品産業全体の構造的問題を解決し、品質の確保された医薬品の安定供給を目指す目的で、「後発医薬品製造基盤整備基金」も新たに創設されました。この基金を利用して、生産性向上のための設備整備を行うなどして、品質の確保された医薬品を安定的に供給できるよう、設備面の整備等を行うのも一案でしょう。
(4)国民への医薬品の適正な提供のための薬局機能の強化
薬剤師等の人材の有効活用と、社会問題化する医薬品の濫用への対策を両立させます。
a 調剤業務の一部外部委託の解禁
薬局開設者が、一包化等の一定の定型的な調剤業務について、薬局の所在地の都道府県知事等の許可を得て、一定の要件を備えた他の薬局の開設者へ委託することを可能としました。当面は同一都道府県内限定の運用とし、今後の検証を踏まえて範囲拡大を検討するとされています(「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律等の一部を改正する法律(令和7年法律第37号)の概要」(厚生労働省ウェブサイト)参照)。外部委託により、対物業務の負担が減ることで、薬剤師が対人業務に集中できる環境が整うことが期待されます。本改正は、公布の日から起算して2年を超えない範囲内(2027年5月20日まで)において政令で定める日に施行されます。
b 薬剤師等が常駐しない店舗における一般用医薬品の販売
委託元の薬剤師等による遠隔での管理の下、あらかじめ登録された薬剤師等が常駐しない店舗(登録受渡店舗)において、医薬品を保管し、購入者へ受け渡すことが可能となりました。例えば、利用者のスマホや受取店舗の販売機等でオンライン服薬指導を経た上で、コンビニエンスストア等のような登録受取店舗で医薬品の受渡しをすることが可能となりました。販売自体は委託元の薬局・店舗販売業者が行い、登録受渡店舗に受渡の委託をする、という建付けであり、原則として委託元の薬局や店舗販売業者が販売に関する責任を有します。本改正は、公布の日から起算して2年を超えない範囲内(2027年5月20日まで)において政令で定める日に施行されます。
c 濫用等のおそれのある医薬品(指定濫用防止医薬品)の販売規制強化等
本改正では、若年者を中心とする一般用医薬品の濫用が社会問題化している状況を踏まえた実効性を高めるための見直しや要指導医薬品に関するデジタル技術を活用したアクセス改善を図る見直し等も含め医薬品の販売区分及び販売方法の見直しが行われました。この見直しの概要は、以下の図のとおりです。
【図:「医薬品の販売区分及び販売方法の見直しの概要(「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律等の一部を改正する法律(令和7年法律第37号)の概要」(厚生労働省ウェブサイト)より抜粋)】

この中でも、特に対応が重要なのが、「指定濫用防止医薬品」の販売に関する改正でしょう。「指定濫用防止医薬品」は、医薬品濫用防止の観点から、濫用をした場合に中枢神経系の興奮又は抑制若しくは幻覚を生ずるおそれがあり、その防止を図る必要がある医薬品を厚生労働大臣が指定するものです。「指定濫用防止医薬品」を販売等する際には、薬局開設者、店舗販売業者又は配置販売業者は、原則として、薬剤師や登録販売者に、当該薬剤や他の薬剤の他の薬局等での購入・使用の状況、(購入者が18歳未満の場合)氏名、年齢、多量購入の場合の理由等の必要な事項を確認させ、書面等により必要な情報を提供させなければなりません。この情報提供ができない場合、指定濫用防止医薬品の販売等が禁止されます。また、大量(大容量)の販売(指定濫用防止医薬品ごとに定める数量を超えた販売)を行う場合や、18歳未満に販売を行う場合には、対面やビデオ通話等での確認が必要です。また、適正な使用を確保できないと認められる場合の販売等や若年者に対する大量の販売等は禁止されます。陳列方法についても、上図のような限定があります。これらの内容も踏まえ、「手順書」を見直し、それに沿った運用を行うことが求められます。本改正に関連し、指定濫用防止医薬品の販売等につき薬局開設者等が対応すべき事項については、「指定濫用防止医薬品の販売等について」(厚生労働省ウェブサイト)が詳しいです。)本改正は、2026年5月1日に施行されます。
Ⅱ 2025年改正薬機法対応簡易チェックリスト
1.経営ガバナンス体制の再点検(2027年5月20日までにおいて政令で定める日施行関係)
2.副作用に係る情報収集等に関する計画(RMP)への対応(2027年5月20日までにおいて政令で定める日施行関係)
3.安定供給体制の整備(2027年5月20日までにおいて政令で定める日施行関係)
4.販売・店舗オペレーション(2026年5月1日施行関係)
本改正による指定濫用防止医薬品の販売方法等については、以下の表もわかりやすいでしょう。
さらに、「手順書」に記載すべき事項をはじめ、本改正に関連し、指定濫用防止医薬品の販売等につき薬局開設者等が対応すべき事項については、「指定濫用防止医薬品の指定について」(厚生労働省ウェブサイト)が詳しいです。「令和7年の医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(薬機法)等の一部改正について」(厚生労働省ウェブサイト)には、他にも、指定濫用防止医薬品の販売等に係る質疑応答集(Q&A)等、指定濫用防止医薬品の適法な販売に重要な情報へのリンクも多数掲載されており、参考になります。
5.最新情報に着目
薬機法のように、企業が対応しなければならない法改正等は、数多くなされており、対応するためには、まず、最新情報に触れることが重要です。最新ニュースや法令の情報等を把握し、折よく対応していくためには、Westlaw Japanがおすすめです。
*このチェックリストは、文中のリンクの他、末尾のリンクを参考に、一部、編集・加工等して作成しています。簡易化のため、適宜省略・加筆等していますので、詳細は下記リンク等をご参照ください。
(掲載日:2026年4月30日)
*この記事は作成・更新時点での情報を基に作成されています。